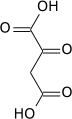
말산

| |

| |
| 이름 | |
|---|---|
| 우선명 (PIN)
2-hydroxybutanedioic acid | |
| 별칭
hydroxybutanedioic acid,
2-hydroxysuccinic acid, L-malic acid, D-malic acid, (–)-malic acid, (+)-malic acid, (S)-hydroxybutanedioic acid, (R)-hydroxybutanedioic acid | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.027.293 |
| EC 번호 |
|
| E 번호 | E296 (방부제) |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C4H6O5 | |
| 몰 질량 | 134.087 g·mol−1 |
| 밀도 | 1.609 g⋅cm−3 |
| 녹는점 | 130 °C (266 °F; 403 K) |
| 558 g/L (at 20 °C)[1] | |
| 산성도 (pKa) | pKa1 = 3.40 pKa2 = 5.20[2] |
| 관련 화합물 | |
다른 음이온
|
말산염 |
관련 카복실산
|
석신산, 타르타르산, 푸마르산 |
관련 화합물
|
뷰탄올, 뷰티르알데하이드, 크로톤알데하이드, 말산 나트륨 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
말산(영어: malic acid) 또는 사과산은 화학식이 C4H6O5 인 유기 화합물이다. 말산은 모든 생물에서 만들어지고, 과일의 유쾌한 신맛에 기여하며, 식품 첨가물로 사용되는 다이카복실산이다. 말산은 2가지 입체 이성질체(L- 및 D-거울상 이성질체)를 갖지만, 자연에 존재하는 형태는 L-이성질체이다. 말산의 염 및 에스터(에스테르)는 말산염(영어: malate)으로 알려져 있으며, 말레이트는 시트르산 회로의 중간생성물이다.
역사 및 어원
[편집] |
말산은 1785년에 칼 빌헬름 셸레에 의해 사과 주스에서 최초로 분리되었다.[3] 앙투안 라부아지에는 1787년에 "acide malique|acide malique"라는 이름을 제안했는데, 이는 "사과"를 뜻하는 라틴어 단어 "mālum"에서 유래되었다(사과나무의 속명은 Malus).[4][5]
음식에서
[편집]말산은 살구, 블랙베리, 블루베리, 체리, 포도, 미라벨 자두, 복숭아, 배, 자두, 마르멜루를 비롯한 많은 과일에서 주요 유기산이며,[6] 감귤류와 같은 다른 과일에는 좀 더 낮은 농도로 존재한다.[7] 말산은 풋사과(덜 익은 사과)의 신맛에 기여한다. 말산은 포도에 존재하며 대부분의 포도주에도 들어있는데 때때로 5 g/L 의 높은 농도로 존재한다.[8] 열매가 성숙해감에 따라 말산의 양은 감소하지만, 말산은 포도주의 시큼한 맛에 기여한다. 말산은 루바브의 기본적인 풍미를 구성한다. 또한 말산은 "소금 & 식초" 맛 감자칩과 같은 일부 인공 식초 맛의 구성 요소이기도 하다.[9]
감귤류에서는 유기농으로 생산된 과일이 일반 농업으로 생산된 과일보다 높은 농도의 말산을 함유하고 있다.[7]
말로락틱 발효(malolactic fermentation) 과정은 말산을 훨씬 더 순한 젖산으로 전환시킨다. 말산은 모든 과일과 많은 채소에서 자연적으로 생성된다.[10]
식품 첨가제로 말산은 E 번호 E296으로 표시된다. 말산은 미국에서 생산되는 과자류에서 강한 신맛을 내는 데에 사용된다. 말산은 시트르산과 함께 신맛이 나는 과자류의 제조에 사용된다. 이러한 신맛이 나는 과자류에는 "과도한 섭취는 입안을 자극할 수 있다"라는 경고 문구가 표시되어 있다. 말산은 유럽 연합,[11] 미국,[12] 오스트레일리아, 뉴질랜드[13]에서 식품 첨가물로 사용하도록 승인되었다.
말산은 섭취시 2.39 kcal/g 의 열량을 낸다.[14]
생화학
[편집]L-말산은 자연적으로 생성되는 형태인 반면, L-말산과 D-말산의 혼합물은 인위적으로 합성할 때 생성된다.
-
L-말산
-
D-말산
말산은 생화학에서 중요한 역할을 한다. C4 탄소고정 과정에서 말산은 캘빈 회로의 CO2공급원이다. 말산은 시트르산 회로의 중간생성물이며, 푸마르산에 하이드록실기(–OH)가 첨가됨으로써 생성된다. 또한 말산은 보충대사 반응을 통해 피루브산으로부터 생성될 수 있다.
말산은 또한 식물 잎의 공변세포에서 포스포엔올피루브산의 카복실화에 의해 합성된다. 말산염은 2가 음이온으로 세포 내의 전하 균형을 유지하기 위해 공변세포로 용질이 유입되는 동안 K+도 같이 수송된다. 공변세포 내에서 이러한 용질의 축적은 용질 퍼텐셜을 감소시키므로 물이 세포 내로 들어가서 기공의 구멍이 확장된다.
한편 말산은 세포질에서 미토콘드리아로 진입할 수 있는 경로를 가지고있는데, 이는 요소 회로와 시트르산 회로의 링크 경로로서 중요하게 다루어진다.
생산 및 주요 반응
[편집]말산의 라세미 혼합물은 말레산 무수물의 이중 수화에 의해 산업적으로 생산된다. 2000년에 미국의 말산 생산 능력은 연간 5000톤이었다. 두 거울상 이성질체는 라세미 혼합물의 키랄 분석에 의해 분리될 수 있고, (S)-거울상 이성질체는 푸마르산의 발효에 의해 특이적으로 얻을 수 있다.[15]
말산과 발연 황산의 자기 축합은 피론 쿠말산을 생성한다.[16]
 |
말산은 발덴 반전(Walden inversion)의 발견 과정에서 중요했으며, 여기서 (−)-말산은 오염화 인의 작용에 의해 (+)-클로로석신산으로 전환된다. 산화 은은 염소 화합물을 (+)-말산으로 전환시킨 다음, PCl5 와 (−)-클로로석신산을 반응시킨다. 산화 은이 이 화합물을 다시 (−)-말산으로 되돌리는 반응으로 전체 반응 사이클이 마무리된다.
같이 보기
[편집]각주
[편집]- ↑ “chemBlink Database of Chemicals from Around the World”. 《chemblink.com》. 2009년 1월 22일에 원본 문서에서 보존된 문서.
- ↑ Dawson, R. M. C. et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ Carl Wilhelm Scheele (1785) "Om Frukt- och Bår-syran" (On fruit and berry acid), Kongliga Vetenskaps Academiens Nya Handlingar (New Proceedings of the Royal Academy of Science), 6 : 17-27. From page 21: " … vil jag hådanefter kalla den Åple-syran." ( … I will henceforth call it apple acid.)
- ↑ de Morveau, Lavoisier, Bertholet, and de Fourcroy, Méthode de Nomenclature Chimique (Paris, France: Cuchet, 1787), p. 108.
- ↑ The Origin of the Names Malic, Maleic, and Malonic Acid Jensen, William B. J. Chem. Educ. 2007, 84, 924. Abstract Archived 2007년 11월 24일 - 웨이백 머신
- ↑ Tabelle I] of “Fruchtsäuren”. 《Wissenschaft Online Lexikon der Biologie》. 2016년 5월 15일에 원본 문서에서 보존된 문서.
- ↑ 가 나 Duarte, A.M.; Caixeirinho, D.; Miguel, M.G.; Sustelo, V.; Nunes, C.; Fernandes, M.M.; Marreiros, A. (2012). “ORGANIC ACIDS CONCENTRATION IN CITRUS JUICE FROM CONVENTIONAL VERSUS ORGANIC FARMING”. 《Acta Horticulturae》 (933): 601–606. doi:10.17660/actahortic.2012.933.78. ISSN 0567-7572.
- ↑ "Methods For Analysis of Musts and Wines", Ough and Amerine, John Wiley and Sons, 2nd Edition, 1988, page 67
- ↑ “The Science Behind Salt and Vinegar Chips”. 《seriouseats.com》.
- ↑ Malic Acid Archived 2018년 6월 25일 - 웨이백 머신, Bartek Ingredients (retrieved 2 February 2012)
- ↑ UK Food Standards Agency: “Current EU approved additives and their E Numbers”. 2011년 10월 27일에 확인함.
- ↑ US Food and Drug Administration: “Listing of Food Additives Status Part II”. 2011년 10월 27일에 확인함.
- ↑ Australia New Zealand Food Standards Code“Standard 1.2.4 - Labelling of ingredients”. 2011년 10월 27일에 확인함.
- ↑ Greenfield, Heather; Southgate, D.A.T. (2003). 《Food composition data: production, management and use》 2판. Rome: Food and Agriculture Organization of the United Nations. 146쪽. ISBN 9789251049495. 2014년 2월 10일에 확인함.
- ↑ Karlheinz Miltenberge (2005), "Hydroxycarboxylic Acids, Aliphatic", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a13_507
- ↑ Richard H. Wiley, Newton R. Smith (1951). “Coumalic acid” 31: 23. doi:10.15227/orgsyn.031.0023.
외부 링크
[편집]- (영어) Malic acid MS Spectrum
- (영어) Calculator: Water and solute activities in aqueous malic acid Archived 2009년 5월 11일 - 웨이백 머신