Ketena
Ketena adalah kelompok senyawa organik yang mengikuti rumus R2C=C=O. Hermann Staudinger adalah pelopor dalam penelitian ketena.[1] Ketena yang paling sederhana adalah ketika kedua gugus R merupakan atom hidrogen, dan nama ketena juga dapat merujuk kepada senyawa ini.

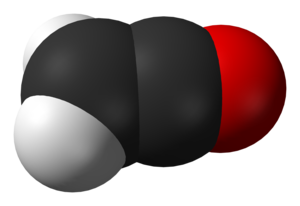
Sifat-sifat
suntingMetil ketena adalah zat tak berwarna, memiliki bau tajam, dan jika terkena manusia dalam konsentrasi pekat, dapat menyebabkan iritasi mata, hidung, tenggorokan, dan paru-paru. Kontak yang cukup lama juga dapat menyebabkan edema pulmonari. Metil ketena memiliki titik lebur -150.5 °C dan titik didih -56.1 °C.
Pembentukan
sunting- Ketena dapat dibuat dari asil klorida melalui sebuah reaksi eliminasi dengan melepaskan HCl
Pembentukan ketena dari asil klorida - Sebuah basa, biasanya trietilamina, melepaskan proton asam di posisi alfa terhadap gugus karbonil, memicu pembentukan ikatan rangkap karbon-karbon dan lepasnya ion klorida.
- Ketena dapat dibentuk melalui reaksi Wolff rearrangement, dari α-diazoketon
- Asam fenilasetat dengan kehadiran basa akan melepaskan air menghasilkan fenilketena, disebabkan keasaman dari proton alfa.
Reaksi
suntingKetena memiliki kereaktifan yang tinggi, dan cenderung menempelkan dirinya ke molekul lain membentuk gugus asetil. Ketena juga dapat bereaksi dengan dirinya sendiri membentuk dimer siklis yang disebut diketena (oksetanon). Ketena juga dapat mengalami reaksi sikloadisi [2+2] dengan alkuna yang kaya elektron membentuk siklobutenon.
Reaksi antara diol (HO-R-OH) dan bis-ketena (O=C=CH-R'-CH=C=O) menghasilkan poliester dengan unit berulang (-O-R-O-CO-R'-CO-).
Lihat pula
suntingReferensi
sunting- ^ Hermann Staudinger (1905). "Ketene, eine neue Körperklasse". Berichte der deutschen chemischen Gesellschaft. 38 (2): 1735–1739. doi:10.1002/cber.19050380283.